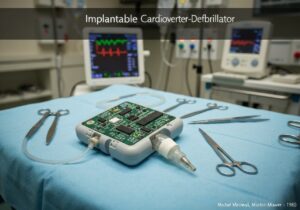
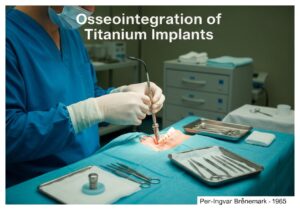
Los dispositivos médicos se clasifican en clases según el riesgo que representan para los pacientes y usuarios. Este enfoque basado en el riesgo, utilizado por organismos reguladores como la FDA de EE. UU. y la UE, suele incluir tres o cuatro niveles (p. ej., Clase I, IIa, IIb, III). Los dispositivos de bajo riesgo, como los depresores linguales, son de Clase I, mientras que los dispositivos de soporte vital de alto riesgo, como los marcapasos, son de Clase III.